Printemps 2025 (Volume 35, numéro 1)
Bilan de l’année : des sciences complexes (et pas si fondamentales)
Par May Y. Choi, MPH, FRCPC
Télécharger la version PDF

Dans le domaine des sciences fondamentales et translationnelles en rhumatologie, les articles de recherche deviennent de plus en plus complexes. Des voies immunitaires complexes aux technologies de pointe utilisées pour étudier nos maladies, comprendre ces découvertes représente un défi, même pour les immunologistes chevronnés. C’est pourquoi, dans ma présentation « Bilan de l’année : sciences fondamentales » lors de l’Assemblée scientifique annuelle (ASA) de 2025 de la Société canadienne de rhumatologie (Calgary, Alberta), j’ai adopté une approche différente. Plutôt que d’expliquer quelles ont été les découvertes les plus marquantes en sciences fondamentales liées à la rhumatologie en 2024, j’ai mis l’accent sur la façon dont ces percées ont été réalisées, en tenant compte de trois grandes tendances récentes : l’intelligence artificielle (IA), le profilage immunitaire et la multiomique.
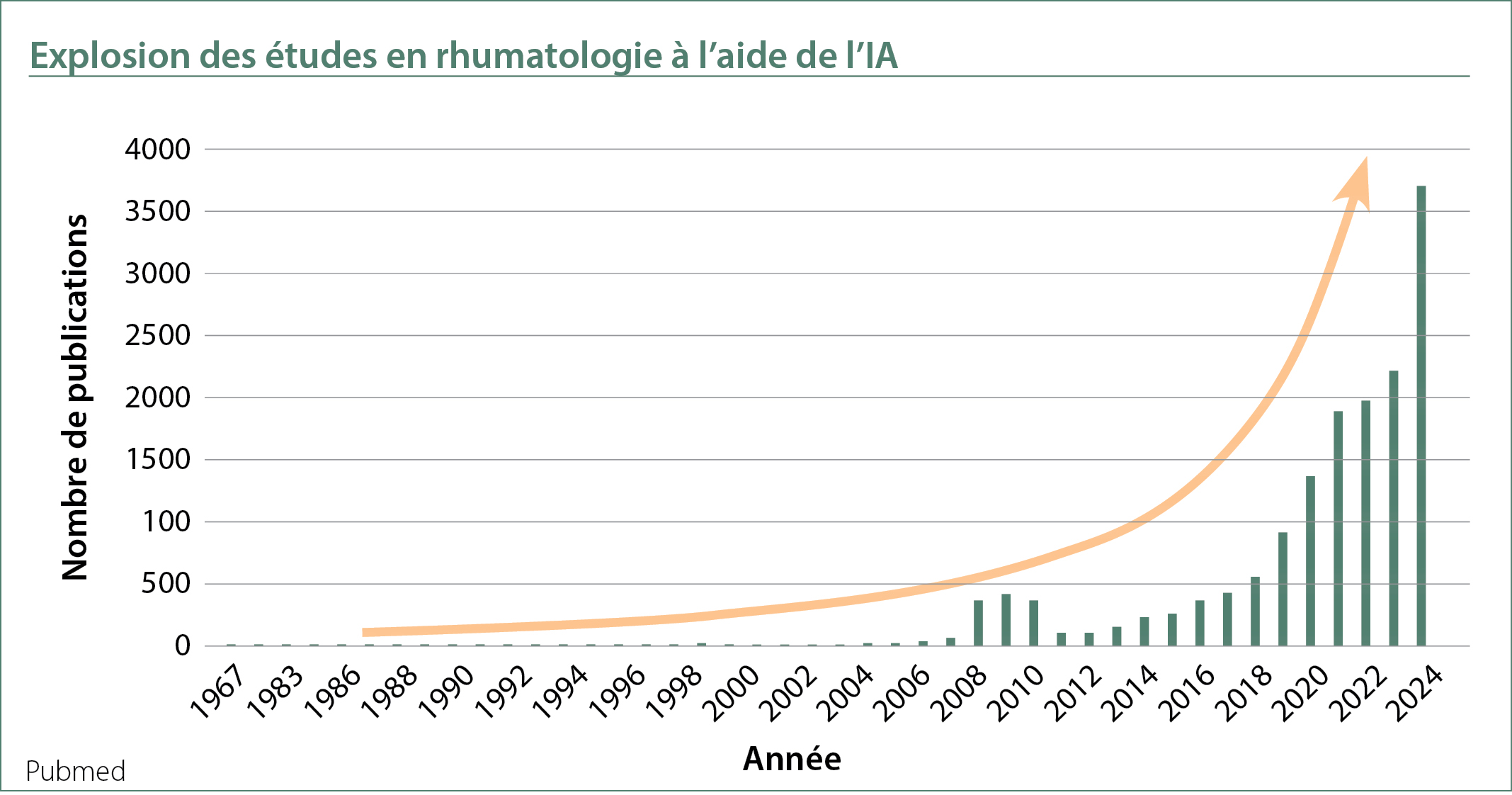
La première technologie clé que j’ai abordée est l’importance croissante de l’intelligence artificielle (IA) en médecine. Bien que le terme intelligence artificielle ait été inventé dans les années 1950, ce n’est que récemment qu’elle a eu un impact majeur sur la recherche en santé, grâce aux progrès du supercalcul et à une meilleure collecte des données des patients, et désormais jusqu’au niveau moléculaire. L’IA est devenue essentielle pour interpréter et intégrer de vastes ensembles de données (big data), permettant de mieux comprendre la physiopathologie des maladies de façon précise et efficace. Elle peut également aider à découvrir de nouveaux schémas qui seraient difficiles à détecter avec les méthodes statistiques traditionnelles. Les algorithmes d’apprentissage automatique, un type d’IA qui inclut l’apprentissage profond (deep learning), peuvent aussi analyser divers types de données, comme des images, du texte et de l’audio.
Dans la recherche sur les maladies auto-immunes, des experts(es) des Instituts nationales de la santé ont tenu une rencontre en 2024 pour définir trois domaines critiques pour la recherche future : l’hétérogénéité des maladies, leur histoire naturelle et le rôle des tissus dans la pathogenèse1. Les biomarqueurs liés à ces aspects sont essentiels pour améliorer notre compréhension des maladies auto-immunes, et l’IA joue un rôle clé dans leur identification. Dans une revue récente des études utilisant l’apprentissage automatique (un type d’IA) dans le lupus, nous avons démontré que l’IA est largement utilisée pour analyser des ensembles de données de biomarqueurs afin d’améliorer la précision diagnostique et de prédire les complications de la maladie2. Ces biomarqueurs incluaient des sous-ensembles de cellules immunitaires (p. ex. cellules T, cellules B) ainsi que des données multiomiques (p. ex. génomique, protéomique, lipidomique). L’association de l’IA avec l’immunophénotypage et les approches multiomiques est devenue une méthode courante en sciences fondamentales pour étudier la pathogenèse des maladies dans notre domaine.
Un flux de travail typique intégrant l’IA, l’immunophénotypage et les approches multiomiques commence par la collecte de biospécimens, comme des échantillons de sang ou de tissu. Ces échantillons sont ensuite analysés pour identifier les sous-types de cellules immunitaires (p. ex. par cytométrie en flux ou de masse) et différentes données omiques (p. ex. séquençage du génome entier, séquençage de l’ARN unicellulaire, spectrométrie de masse). Les données obtenues forment généralement un vaste ensemble de biomarqueurs, qui est ensuite analysé par des algorithmes d’apprentissage automatique afin de repérer des schémas et des biomarqueurs potentiels pour la stratification des patients, le diagnostic, le pronostic, la compréhension de la pathogenèse des maladies et l’identification de nouvelles cibles thérapeutiques.
En ce qui concerne l'avenir proche, il y a une volonté de développer des modèles d’IA encore plus grands, capables de traiter un nombre accru de paramètres et de connexions entre leurs « neurones ». Pour donner un ordre de grandeur, le cerveau humain possède environ 100 000 milliards de connexions, tandis que des modèles comme ChatGPT en utilisent environ 1 000 milliards3. Étant donné la croissance exponentielle des applications de l’IA, il ne serait pas surprenant que ces modèles atteignent bientôt ce seuil. D’autres technologies prometteuses sont aussi à surveiller, notamment la protéomique spatiale, désignée Méthode de l’année par Nature4. Cette technique pousse les approches omiques encore plus loin en fournissant une cartographie spatiale de l’expression des protéines dans les tissus. Elle pourrait révolutionner la manière dont les chercheur(-se)s étudient les maladies à partir de biopsies tissulaires, comme celles du synovium, des muscles, des reins ou de la peau, en offrant une vision plus complète du système immunitaire. Après tout, une image vaut mille mots! Cette méthode ouvre la porte à des traitements plus personnalisés et à une compréhension plus approfondie des mécanismes des maladies, créant ainsi de nouvelles perspectives de recherche et améliorant les soins en rhumatologie.
May Y. Choi, M.D., MPH, FRCPC
Professeure agrégée,
Cumming School of Medicine
Université de Calgary et
Alberta Health Services
Calgary (Alberta)
Références :
1. Guerau-de-Arellano M, Morris MA, Sherman MA, Esch TR. Meeting report: Hidden links in autoimmunity. Science Immunology. 2024;9(102):eads5884.
2. Zhan K, Buhler KA, Chen IY, Fritzler MJ, Choi MY. Systemic lupus in the era of machine learning medicine. Lupus Science & Medicine. 2024;11(1):e001140.
3. Ananthaswamy A. In AI, is bigger always better? Nature. 2023;615(7951):202-5.
4. Karimi E, Simo N, Milet N, TE W, ALSH A, QU N, et al. Method of the Year 2024: spatial proteomics. Nat Methods. 2024;21:2195-6.
|
