Automne 2014 (volume 24, numéro 3)
Lignes directrices pour la PR : Pratiques des rhumatologues du Canada par rapport aux
recommandations de la SCR pour le traitement de la PR (6e partie)
par Sankalp V. Bhavsar, M.D., FRCPC,
au nom de Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC, Vivian P. Bykerk, M.D., FRCPC, Glen S. Hazlewood, M.D., FRCPC, Pooneh Akhavan, M.D., FRCPC, Orit Schieir, M.Sc.,
et Sanjay Dixit, M.D., FRCPC
Télécharger le PDF
Dans ce sixième et dernier volet, nous vous présentons les résultats des questions du sondage portant sur les affections malignes.
1. Un patient atteint de polyarthrite rhumatoïde (PR) recevant
de l’étanercept et du méthotrexate (MTX) en traitement d’entretien présente maintenant un cancer des poumons nouvellement diagnostiqué et commencera bientôt un traitement de radiothérapie et chimiothérapie. Quelle serait votre recommandation à l’égard de l’étanercept?
Réponse : Interrompre l’étanercept.
Recommandation/preuve à l’appui : non applicable; recommandation unanime.
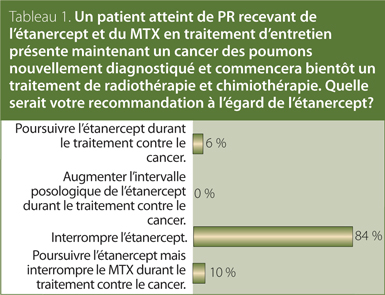
Aucune preuve identifiée n’aborde la question de l’utilisation des antirhumatismaux modifiant l'évolution de la maladie (ARMM) traditionnels ou biologiques chez les patients atteints de PR présentant une affection maligne active. La recommandation de la SCR est qu’en général, le traitement par des ARMM traditionnels ou biologiques des patients atteints de PR présentant une affection maligne active devrait être retardé ou interrompu pendant le traitement de chimiothérapie ou de radiothérapie. Il convient de prendre les décisions thérapeutiques au cas par cas, en consultation avec un oncologue et le patient.
2. Un patient atteint de PR a des antécédents de lymphome. Vous envisageriez tous les traitements suivants, sauf :
Réponse : l’infliximab.
Recommandation/preuve à l’appui : non applicable; recommandation unanime.
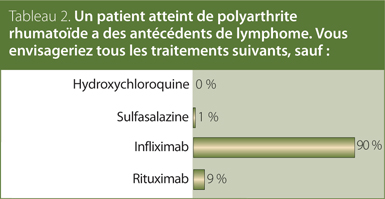
MTX/ARMM : Une étude cas-témoins s’est penchée sur le risque de lymphome incident (pas récidivant) chez les patients atteints de PR traités par le MTX par rapport aux patients atteints de PR traités par d’autres ARMM; cette étude a signalé une légère hausse du risque avec le MTX, mais qui n’était toutefois pas statistiquement significative (RR : 1,23; IC à 95 % : 0,97 à 1,57). Dans cette étude, l’utilisation de léflunomide, de sulfasalazine, d’agents antipaludiques ou d’or n’a pas été associée à une hausse du risque de lymphome. Quatre études ont examiné les risques de maladie lymphoproliférative chez les patients atteints de PR traités par le MTX ou d’autres ARMM comparativement à la population générale; toutes ont démontré un risque plus élevé (lymphome non hodgkinien : ratio standardisé d'incidence [RSI] = 5,1, IC à 95 % : 2,2 à 10; RSI = 5,4, IC à 95 % : 1,1 à 15,7; toute maladie lymphoproliférative : RSI = 3,8, IC à 95 % : 2,2 à 6,2; lymphome : RSI = 1,7, IC à 95 % : 0,9 à 3,2).
Agents biologiques : Une méta-analyse du réseau Cochrane des essais à répartition aléatoire examinant l’innocuité de la thérapie biologique (à l’exclusion du tocilizumab) n’a pas observé de hausse du risque de lymphome avec un ou l’autre des agents biologiques (RC : 0,53; IC à 95 % : 0,17 à 1,66), mais les données étaient toutefois limitées à très peu d’événements. De même, quatre études observationnelles ont examiné le risque de lymphome chez des patients atteints de PR traités par des agents inhibiteurs du facteur de nécrose tumorale (TNF) par rapport à des patients atteints de PR n’ayant jamais reçu d’agents biologiques; aucune de ces études n’a démontré un risque accru associé aux agents anti-TNF, mais sans possibilité de conclusions définitives en raison des faibles incidences de malignités et du manque de précision entourant les estimations des études (risque relatif : 1,4; IC à 95 % : 0,8 à 2,1; rapport des risques : 1,1; IC à 95 % : 0,5 à 2,4; RC : 1,0; IC à 95 % : 0,6 à 1,8 et rapport des risques : 5,0; IC à 95 % : 0,9 à 27,9). Huit études ont signalé une hausse du risque de lymphome chez les patients atteints de PR traités par des agents anti-TNF par rapport à la population générale, dont une étude qui signalait un risque plus élevé avec l’adalimumab ou l’infliximab par rapport à l’étanercept (adalimumab : RC : 4,7, IC à 95 % : 1,3 à 17,7; infliximab : RC : 4,1, IC à 95 % : 1,4 à 12,5). Dans une prolongation ouverte d’un essai contrôlé avec répartition aléatoire, aucune hausse du risque de lymphome n’a été observée chez les patients atteints de PR traités par l’abatacept par rapport aux patients atteints de PR traités par des ARMM traditionnels.
La recommandation de la SCR stipule que l’hydroxychloroquine, la sulfasalazine et le rituximab peuvent être utilisés chez les patients atteints de PR présentant des antécédents de lymphome. Les agents anti-TNF ne sont pas recommandés et les autres ARMM traditionnels et biologiques devraient être utilisés avec prudence.
3. Un patient atteint de PR a déjà été traité pour un cancer colorectal et est en rémission depuis 11 ans. Parmi les choix ci-dessous, quelles sont les options de traitement possibles pour ce patient?
Réponse : Toutes ces réponses.
Recommandation/preuve à l’appui : non applicable; recommandation unanime.
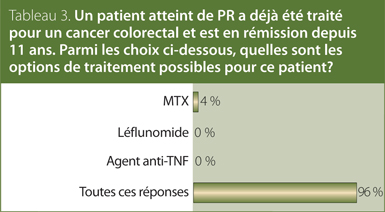
MTX/ARMM : Le traitement par des ARMM traditionnels spécifiques n’a pas été associé à une hausse significative du risque de cancer des poumons dans une étude cas-témoins à l’intérieur d’une base de données de réclamations administratives. Deux études ont signalé une hausse du risque de cancer des poumons chez les patients atteints de PR traités par le MTX par rapport à la population générale (RSI : 2,9, IC à 95 % : 1,6 à 4,8; et RSI : 3,5, IC à 95 % : 1,4 à 7,1), dont une qui signalait également un risque plus élevé de mélanome (RSI : 3,0, IC à 95 % : 1,2 à 6,2).
Agents biologiques : Les patients atteints de PR traités par des agents anti-TNF n’ont pas présenté un risque accru de tumeurs solides par rapport aux patients atteints de PR traités par un ARMM traditionnel dans quatre études, mais une étude a signalé un risque accru de mélanome avec l’infliximab (RC : 2,6, IC à 95 % : 1,0 à 6,7) et l’étanercept (RC : 2,4, IC à 95 % : 1,0 à 5,8). Le traitement anti-TNF n’a pas été associé à un risque accru de tumeurs solides par rapport à la population générale dans trois études; cependant, dans une analyse de types spécifiques de tumeurs solides, une étude a signalé un risque accru de cancer des poumons et une étude distincte a signalé une tendance non significative vers un risque accru pour les cancers associés au tabagisme (RSI : 2,2; IC à 95 % : 0,7 à 5,1). Une hausse du risque de cancers associés au tabagisme et une baisse du risque de cancer du sein ont également été signalées chez les patients atteints de PR non traités par des agents anti-TNF par rapport à la population générale. L’abatacept n’a pas été associé à un risque accru de tumeurs solides par rapport aux patients atteints de PR traités par des ARMM traditionnels ou par rapport à la population générale dans une étude de prolongation ouverte.
La recommandation de la SCR est que les ARMM traditionnels peuvent être utilisés chez les patients atteints de PR présentant des antécédents de malignité solide. Les ARMM biologiques devraient être utilisés avec prudence.
Pour de plus amples renseignements à propos de ces recommandations et des données probantes appuyant ces résultats, veuillez consulter les lignes directrices de la SCR concernant la PR, disponible à l’adresse www.rheum.ca/fr/publications/cra_ra_guidelines. Vous pouvez consulter les volets précédents de ces lignes directrices sur le site craj.ca.
Sankalp Bhavsar, M.D., FRCPC
Boursier en rhumatologie,
Université McMaster,
Hamilton, Ontario
au nom de : Carter Thorne, M.D., FRCPC, FACP,
Claire Bombardier, M.D., FRCPC,
Vivian P. Bykerk, M.D., FRCPC,
Glen S. Hazlewood, M.D., FRCPC,
Pooneh Akhavan, M.D., FRCPC,
Orit Schieir, M.Sc., et
Sanjay Dixit, M.D., FRCPC |



