Hiver 2013 (volume 23, numéro 4)
La capillaroscopie en rhumatologie
par Geneviève Gyger, M.D., FRCP, et
Marie Hudson, M.D., FRCPC
Télécharger le PDF
Une femme âgée de 40 ans est orientée à la clinique de rhumatologie pour une capillaroscopie périunguéale. Hormis la présence du phénomène de Raynaud depuis 10 ans, la patiente ne présente aucun antécédent médical pertinent; elle ne fume pas. Elle a trois enfants en santé et n’a subi aucune fausse-couche. Elle ne prend aucun médicament. Les antécédents familiaux ne révèlent rien de particulier et montrent qu’il n’y a aucun antécédent du phénomène de Raynaud dans la parenté. À l’interrogatoire, la patiente déclare qu’elle ne souffre pas de brûlures gastriques, d’essoufflement, d’arthrite et qu’elle ne manifeste aucun autre symptôme d’une atteinte du tissu conjonctif. L’examen physique confirme l’absence de sclérodactylie, du signe de la nuque, de plis péribuccaux plus marqués et d’épaississement de la peau; en revanche, l’examen met en évidence deux télangiectasies sur la face interne de la lèvre inférieure. La recherche d’anticorps anti-antigène nucléaire soluble (ENA, pour extractible nuclear antigen), y compris les anticorps anti-topoisomérase I a été négative. Par contre, la vidéocapillaroscopie périunguéale (DS Medica, grossissement x200) a montré un aspect caractéristique d’une sclérodermie active (Figure 1).
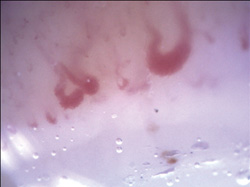
Figure 1. Les capillaires géants sont le signe cardinal des anomalies typiques dans la sclérodermie. La présence même d’un seul capillaire géant est toujours anormale et elle est caractéristique de la sclérodermie. À ce signe distinctif s’ajoutent les ectasies, les hémorragies capillaires, la perte de capillaires, la néoangiogenèse et la désorganisation. Plus de 95 % des patients atteints de ScG présenteront ces anomalies typiques à la vidéocapillaroscopie. On peut voir sur cette image deux capillaires géants, une hémorragie et une densité capillaire légèrement amoindrie.
Cette patiente est-elle atteinte de sclérodermie?
D’après des études épidémiologiques, la fréquence du phénomène de Raynaud est de l’ordre de 2 à 22 % et dans environ 15 % de ces cas, ce trouble est associé à la sclérodermie généralisée (ScG)1,2. Parmi les personnes qui manifestent le phénomène de Raynaud, lesquelles sont susceptibles d’être tôt ou tard atteintes de ScG? Une étude prospective menée durant 20 ans auprès de 586 patients atteints du phénomène de Raynaud a montré que des anomalies détectées à la capillaroscopie périunguéale de référence, couplées à la présence d’auto-anticorps spécifiques de la ScG (anti-protéine B du centromère [CENP-B, pour centromere protein B], anti-topoisomérase I, anti-Th/To, ou anti-ARN-polymérase III), se sont révélées d’excellents prédicteurs de la constitution d’une ScG, alors que l’absence de ces facteurs permettait pratiquement d’écarter une telle issue. En effet, les patients qui manifestaient ces deux anomalies au début de l’étude avaient un risque 60 fois plus élevé d’être atteints tôt ou tard de ScG, comparativement au groupe témoin (sans ces anomalies); 80 % des patients porteurs des deux anomalies ont été atteints de ScG au cours des 20 années de suivi. À l’opposé, seulement 2 % des patients atteints du phénomène de Raynaud qui avaient obtenu des résultats normaux à la capillaroscopie de référence et ne portaient pas d’auto-anticorps spécifiques de la ScG au début de l’étude ont été atteints d’une ScG caractérisée durant la période de suivi2.
Cette étude pivot2 a validé les critères proposés par Leroy et Medsger3 en 2001 pour évaluer la ScG au stade précoce; ces critères comprenaient le phénomène de Raynaud, les auto-anticorps spécifiques de la ScG (anti-centromère, anti-topoisomérase I, anti-fibrillarine, anti PM/Scl ou anti-ARN polymérase I ou III), ainsi que des résultats caractéristiques de la sclérodermie à la capillaroscopie. L’application de ces critères a fait bondir le taux de sensibilité des critères prélimi-naires de 1980 de l’American College of Rheumatology (ACR)4 pour la sclérodermie circonscrite de 33 à 92 %5. Nous devrions néanmoins garder à l’esprit que 20 % des patients qui remplissent ces critères ne seront pas atteints de ScG, à tout le moins durant un suivi de 20 ans.
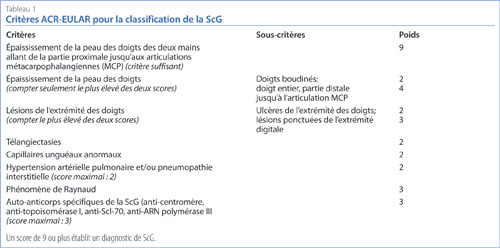
En 2012, l’ACR et l’European League Against Rheumatism (EULAR) ont créé conjointement un comité chargé d’élaborer de nouveaux critères de classification de la ScG (Tableau 1)6. Ces critères ont été élargis pour inclure des anomalies capillaires périunguéales. Un score de 9 ou plus établit un diagnostic de ScG. La patiente de l’étude de cas présentée ci-dessus remplit les critères du diagnostic définitif de ScG selon les nouveaux critères ACR-EULAR. Elle est atteinte du phénomène de Raynaud (2 points), elle porte des auto-anticorps anti-centromère (3 points), elle présente des signes de ScG à la capillaroscopie (2 points) ainsi que des télangiectasies (2 points), ce qui porte le total de points à 9. On voit donc que la capillaroscopie s’est révélée un outil fort utile pour poser le diagnostic de ScG chez cette patiente.
Bilan proposé
La prochaine étape de l’évaluation devrait viser à déterminer si des organes internes sont touchés, notamment à l’aide des examens suivants : une étude du transit œsophagien ou transit baryté pour écarter la dysmotilité œsophagienne; une échocardiographie pour mesurer les pressions artérielles pulmonaires; une radiographie pulmonaire et des épreuves de la fonction pulmonaire pour écarter une pneumopathie interstitielle. On pourrait aussi envisager une radiographie des mains pour rechercher une calcinose ou une acro-ostéolyse. Chez cette patiente, le bilan n’a pas montré d’anomalies, sauf les résultats de l’étude du transit œsophagien qui évoquent une dysmotilité œsophagienne modérée.
Traitement
Le traitement du phénomène de Raynaud reste fondé sur la maîtrise des symptômes. Au nombre des interventions non pharmacologiques, on note l’abandon du tabac, le port de vêtements chauds et l’évitement maximal de l’exposition au froid. Les antagonistes du calcium conviennent au traitement de première intention lorsqu’on envisage une pharmacothérapie7. On devrait envisager de prescrire un inhibiteur de la pompe à protons (IPP), même chez des patients sans symptômes, pour prévenir les complications du reflux gastro-œsophagien. Ces complications peuvent comprendre une œsophagite, des rétrécissements de l’œsophage et l’œsophage de Barett. L’importance de traiter énergiquement la dysmotilité œsophagienne a été mise en évidence par des études récentes ayant montré une relation entre la micro-aspiration asymptomatique secondaire au reflux d’acide gastrique et la pneumopathie interstitielle dans la SG8,9. Fait à noter, 70 à 90 % des patients atteints de ScG manifestent un trouble œsophagien, et dans 50 % de ces cas, ce trouble est asymptomatique7.
Conclusion
La capillaroscopie périunguéale est un examen rapide, non effractif et facile à réaliser qui devrait faire partie de l’évaluation des personnes atteintes du phénomène de Raynaud, ainsi que pour faciliter le diagnostic de la sclérodermie généralisée et pour rassurer les patients qui ne sont pas porteurs d’auto-anticorps et dont la circulation capillaire est normale. Les appareils pouvant être utilisés pour la capillaroscopie périunguéale comprennent le dermatoscope (grossissement x10), l’ophtalmoscope (x20), le microscope grand champ (x50) et le vidéocapillaroscope (x20). Même si le dermatoscope et l’ophtalmoscope sont disponibles à la clinique, la meilleure résolution offerte par le microscope grand champ et par la vidéocapillaroscopie permet d’identifier plus efficacement toutes les caractéristiques vasculaires de la ScG. Par ailleurs, la valeur diagnostique et pronostique de la capillaroscopie dans les autres maladies rhumatologiques est encore à l’étude, en particulier dans les myosites dans lesquelles on a décrit des caractéristiques semblables à celles de la sclérodermie. Aucune caractéristique spécifique d’autres maladies du tissu conjonctif n’a été décrite. Dans ces maladies, la détection de caractéristiques évoquant la ScG laisse croire à un chevau-chement avec la ScG.
Références :
1. Spencer-Green G. Outcomes in primary Raynaud phenomenon: a meta-analysis of the frequency, rates, and predictors of transition to secondary diseases. Arch Intern Med 1998; 158(6):595-600.
2. Koenig M, Joyal F, Fritzler MJ, et coll. Autoantibodies and microvascular damage are independent predictive factors for the progression of Raynaud's phenomenon to systemic sclerosis: a twenty-year prospective study of 586 patients, with validation of proposed criteria for early systemic sclerosis. Arthritis Rheum 2008; 58(12):3902-12.
3. LeRoy EC & Medsger TA Jr. Criteria for the classification of early systemic sclerosis. J Rheumatol 2001; 28(7):1573-6.
4. Preliminary criteria for the classification of systemic sclerosis (scleroderma). Subcommittee for scleroderma criteria of the American Rheumatism Association Diagnostic and Therapeutic Criteria Committee. Arthritis Rheum 1980; 23(5):581-90.
5. Lonzetti LS, Joyal F, Raynauld JP, et coll. Updating the American College of Rheumatology preliminary classification criteria for systemic sclerosis: addition of severe nailfold capillaroscopy abnormalities markedly increases the sensitivity for limited scleroderma. Arthritis Rheum 2001; 44(3):735-6.
6. Van den Hoogen F, Khanna D, Fransen J, et coll. Classification criteria for systemic sclerosis: An ACR-EULAR Collaborative Initiative. Arthritis Rheum 2013 (conditionally accepted).
7. Herrick AL. Contemporary management of Raynaud's phenomenon and digital ischaemic complications. Curr Opin Rheumatol 2011; 23(6):555-61.
8. Savarino E, Bazzica M, Zentilin P, et coll. Gastroesophageal reflux and pulmonary fibrosis in scleroderma: a study using pH-impedance monitoring. Am J Respir Crit Care Med 2009; 179(5):408-13.
9. Christmann RB, Wells AU, Capelozzi VL, et coll. Gastroesophageal reflux incites interstitial lung disease in systemic sclerosis: clinical, radiologic, histopathologic, and treatment evidence. Semin Arthritis Rheum 2010; 40(3):241-9.
Geneviève Gyger, M.D., FRCPC
Professeure adjointe de médecine,
Université McGill
Division de rhumatologie,
Hôpital général juif
Montréal, Québec
Marie Hudson, M.D., M.P.H., FRCPC
Professeure adjointe de médecine,
Université McGill
Division de rhumatologie,
Hôpital général juif
Institut Lady Davis de recherches médicales
Montréal, Québec |



